Wie wirken Antibiotika?
Antibiotika sind (meist verschreibungspflichtige) Medikamente, die krankmachende Bakterien abtöten oder deren Wachstum verhindern. Sind Bakterien in den Körper eingedrungen und vermehren sich, können sie eine Entzündung auslösen. Die Wirksamkeit von Antibiotika beschränkt sich auf bakterielle Infektionen. Wenn die Infektion allerdings durch Viren verursacht wurde, was bei Magen-Darm-Beschwerden und Erkältungen häufig der Fall ist, sind Antibiotika wirkungslos.
Der grosse Nachteil von Antibiotika besteht darin, dass sie nicht nur gegen schädliche Erreger wirken, sondern auch die nützlichen Bakterien schwächen oder eliminieren. Daher sollte Antibiotika nur dann verschrieben und eingesetzt werden, wenn es wirklich notwendig ist.
Was muss ich bei der Einnahme von Antibiotika beachten?
Der menschliche Körper ist mit Tausenden verschiedenen Bakterienarten besiedelt. Ein Bakterien-Gleichgewicht ist für unseren Körper unerlässlich. Mit einer Antibiotika-Behandlung wird allerdings dieses Gleichgewicht gestört. Denn die Antibiotika wirken nicht nur gegen Krankheitserreger, sondern auch gegen nützliche Bakterien. Nützliche Bakterien sind solche die uns helfen, Nahrung zu verdauen oder entzündungslindernde Substanzen herzustellen.
Weiterhin ist es wichtig zu wissen, dass die Einnahme von Antibiotika mit Nebenwirkungen einhergehen kann. Am häufigsten kommen dabei Durchfall, Übelkeit, Magen-Darm-Probleme und allergische Reaktionen der Haut vor. Welche Nebenwirkungen genau und wie stark auftreten ist sehr individuell.
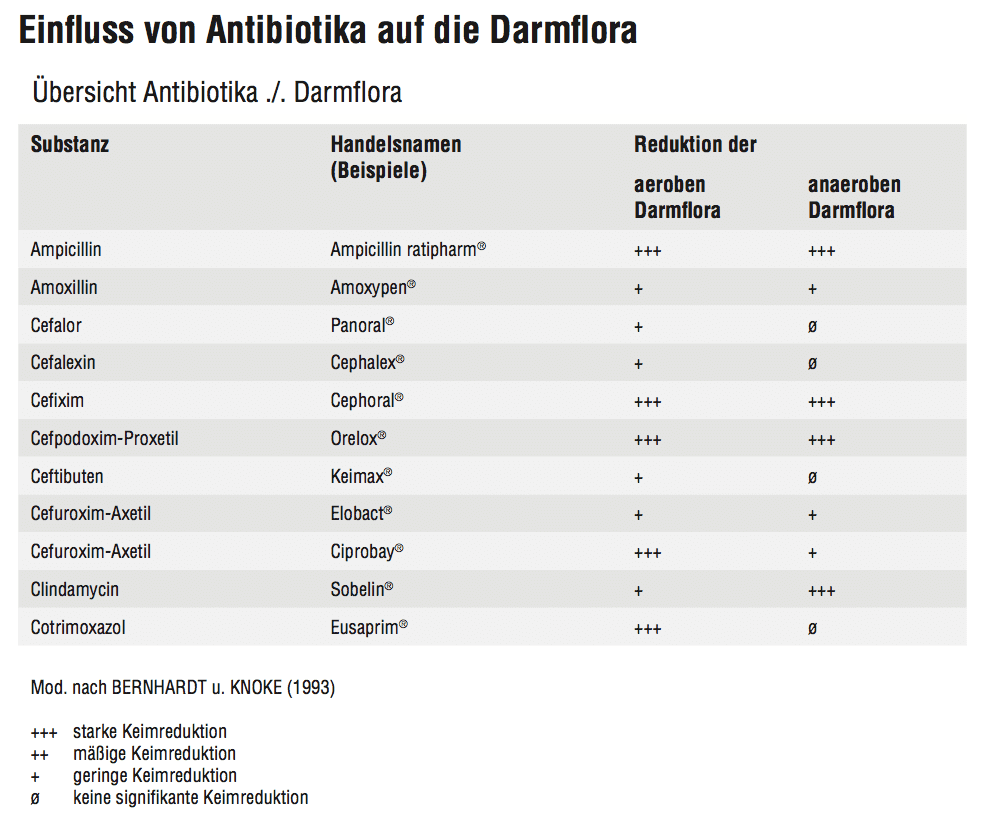
Einfluss von Antibiotika auf die Darmflora
Antibiotika heisst übersetzt „gegen das Leben“, weil Bakterien abgetötet werden. Was kommt aber danach? Wenn wir eine Antibiotika-Kur gemacht haben sind nicht nur die Bakterien tot, sondern auch das ganze Darm-Milieu verändert sich.
Der pH-Wert im Darm, der zwischen 6-6.5 liegen sollte, verschiebt sich Richtung 7 und mehr. Dies hingegen fördert die Ansiedlung von Pilzen. Deshalb passiert es vielen Personen nach einer Antibiotika-Einnahme, dass sie plötzlich Ausschläge bekommen oder Frauen auch sehr oft eine Blasenentzündung.
Damit man sich das ungefähr vorstellen kann, versuche ich es mal mit einem Beispiel aus der Natur: Wenn in stehendem Gewässer der pH-Wert zu basisch wird, bekommt ein Teich Algen und ein Pool kippt, wird trübe. Die meisten geben dann pH Down und/oder Chlor dazu. Um den pH-Wert wieder etwas nach unten zu bringen, Richtung sauer. Bei einem Teich geben heute immer mehr Leute EM Produkte ins Wasser, um den pH-Wert zu verbessern. EM sind sogenannte Effektive Mikroorganismen oder anders gesagt Milchsäurebakterien.
Das würde also bedeuten, wenn wir unseren pH-Wert wieder verbessern möchten, könnten wir ebenfalls mit diesen Methoden arbeiten. Milchsäurebakterien kommen leider nicht mehr allzu häufig in unserer Nahrung vor, am bekanntesten noch in fermentierter Nahrung wie zum Beispiel Sauerkraut.
Supplemente nach einer Antibiotika Therapie
Nach einer Antibiotika Therapie kann die Darmflora durch die Einnahme von Supplementen wieder aufgebaut werden. Dafür eignen sich besonders gut Milchsäurebakterien, also probiotische, nützliche Bakterien.
Vor, während und nach der Antibiotika-Therapie empfehlen wir besonders unsere Probiotikum Kapseln ARKTIBIOTIC Akut.
Hochdosierte Milchsäurebakterien und zusätzlich wertvolles Vitamin D enthält das ARKTIBIOTIC Premium.
Die Historie von Antibiotika
Antibiotika gehören zweifellos zu den grössten Errungenschaften der Medizin. Die meisten unter uns können sich nicht an eine Zeit erinnern, in der sie nicht zur Verfügung gestanden hätten. In einer Welt ohne Antibiotika, könnte der kleinste Kratzer den Tod bedeuten, wären Operationen ungleich gefährlicher und manche gar nicht möglich, und Risikopatienten mit chronischen Erkrankungen oder Menschen, die Transplantationen oder Gelenkersatz hinter sich haben wären extrem gefährdet. Wir haben auch vergessen, wie selten es für Eltern war, alle ihre Kinder das Erwachsenenalter erreichen zu sehen.
Schon seit dem 17. Jahrhundert weiss man um die Existenz von Mikroorganismen. Ihre Entdeckung verdanken wir dem Einfallsreichtum von Robert Hooke und Antoni van Leeuwenhoek, denen es durch die Herstellung und Verwendung einfacher Mikroskope gelungen war, Objekte etwa 25- bis 250-fach zu vergrössern. [1] Dennoch dauerte es noch über 200 Jahre ehe Mikroorganismen als Krankheitserreger wahrgenommen wurden. Bis dahin glaubten die Menschen, dass üble Gerüche Krankheiten verursachen können oder dass böse Geister einen Menschen krank machen können.
Gegen Ende des 19. Jahrhundert entdeckte Robert Koch, dass ein bestimmter Keim eine bestimmte Krankheit verursachen kann. Der Beweis der «Keimtheorie» war die Leistung von Louis Pasteur. Wie Robert Koch war er der Meinung, dass Krankheiten durch mikroskopische Organismen verursacht werden, aber diese Ansicht war im 19. Jahrhundert umstritten und stellte sich gegen die akzeptierte Theorie der «spontanen Entstehung». Die Theorie der spontanen Entstehung ging davon aus, dass Lebewesen aus unbelebter Materie entstehen können und dass solche Prozesse alltäglich sind und regelmässig stattfinden.
So wusste man nun also, dass Bakterien krank machen können, es gab aber keine Möglichkeit, dies zu verhindern. Durch «Pasteurisierung» – das Erhitzen von Flüssigkeiten wie Wasser und Milch – konnten Bakterien abgetötet werden. Dank der Beobachtungen von Dr. Sauerbruch in Wien zeigte sich, dass Sauberkeit und Händewaschen das Risiko der Übertragung und Ausbreitung von Krankheiten wesentlich reduzierten. Diese Massnahmen bedeuteten, dass viele Erkrankungen vermieden werden konnten. Hatte eine Infektion jedoch bereits stattgefunden, konnte man nur noch auf die Selbstheilungskräfte des Patienten – also die Wirkung des Immunsystems – hoffen.
Dabei waren Antibiotika nicht gänzlich unbekannt. Die Behandlung mikrobieller Infektionen im alten Ägypten, Griechenland und China ist gut dokumentiert. [2] Die moderne Ära der Antibiotika begann mit der Entdeckung von Penicillin durch Sir Alexander Fleming im Jahr 1928. Antibiotika wurden erstmals in den 1940er Jahren zur Behandlung schwerer Infektionen verschrieben. [3]
Seitdem haben Antibiotika die moderne Medizin verändert und Millionen von Menschenleben gerettet, doch schon in den 1950er Jahren waren viele der Fortschritte des vorangegangenen Jahrzehnts gefährdet. Es traten bereits Resistenzen gegen Penicillin auf. Als Reaktion darauf wurden neue Beta-Lactam-Antibiotika entdeckt, entwickelt und eingesetzt, wodurch das Vertrauen in Antibiotika wiederhergestellt werden konnte. Im selben Jahrzehnt wurde jedoch der erste Fall von Methicillin-resistentem Staphylococcus aureus (MRSA) identifiziert: 1962 in Grossbritannien und 1968 in den Vereinigten Staaten.
Heute sterben laut WHO jedes Jahr mindestens 700.000 Menschen an arzneimittelresistenten Krankheiten, darunter 230.000 an multiresistenter Tuberkulose. Immer mehr verbreitete Krankheiten, darunter Atemwegsinfektionen, sexuell übertragbare Infektionen, Darminfektionen und Harnwegsinfektionen, sind unbehandelbar; lebensrettende medizinische Verfahren werden immer riskanter. [4]
Quelle: Pexels
Wie kommt es zu Antibiotika-Resistenzen?
Epidemiologische Studien haben einen direkten Zusammenhang zwischen dem Antibiotikakonsum und der Entstehung und Verbreitung resistenter Bakterienstämme nachgewiesen. [5] Unter Bakterien können nicht nur Gene von Verwandten vererbt, sondern auch von Nichtverwandten erworben werden. Dieser sogenannte «horizontale Gentransfer» kann die Übertragung von Antibiotikaresistenzen zwischen verschiedenen Bakterienarten ermöglichen. Ausserdem können Resistenzen spontan durch Mutation auftreten. [6] Antibiotika entfernen einen Grossteil der bakteriellen «Konkurrenz». Was zurückbleibt sind resistente Bakterien, die sich dann ungestört als Ergebnis natürlicher Selektion vermehren können.
Obwohl bereits seit Jahrzehnten vor übermässigem Gebrauch gewarnt wird, werden Antibiotika weltweit überverschrieben. [7] In vielen Ländern sind Antibiotika sogar unreguliert und rezeptfrei erhältlich. Dieser Mangel an Regulierung führt zu Antibiotika, die leicht zugänglich, reichlich und billig sind, was einen übermässigen Gebrauch begünstigt. Die Möglichkeit, solche Produkte online zu kaufen, hat sie auch in Ländern zugänglich gemacht, in denen Antibiotika offiziell reguliert sind.
Auch falsch verschriebene Antibiotika tragen zur Förderung resistenter Bakterien bei. Studien haben gezeigt, dass die Behandlungsindikation, die Wahl des Mittels oder die Dauer der Antibiotikatherapie in 30 bis 50 % der Fälle falsch ist. [8]
Resistenzen sind nicht nur auf Überkonsum in der Humanmedizin zurückzuführen. Der wahrscheinlich grössere Teil der Antibiotika wird sowohl in den Industrieländern als auch in den Entwicklungsländern in grossem Umfang als Wachstumszusätze bei Vieh verwendet. Geschätzte 80 % der in den USA verkauften Antibiotika werden bei Tieren eingesetzt, in erster Linie zur Wachstumsförderung und zur Verhinderung von Infektionen. [9], [10] Die Behandlung von Vieh mit antimikrobiellen Mitteln soll die allgemeine Gesundheit der Tiere verbessern und zu grösseren Erträgen und einem ‚hochwertigeren‘ Produkt führen. Die bei Nutztieren verwendeten Antibiotika werden vom Menschen mit der Nahrung aufgenommen. [11] Die Übertragung resistenter Bakterien auf den Menschen durch Nutztiere wurde erstmals vor mehr als 35 Jahren festgestellt, als hohe Raten von Antibiotikaresistenzen in der Darmflora sowohl von Nutztieren als auch von Landwirten gefunden wurden.

Quelle: Unsplash
In der Schweiz ist der Einsatz von Antibiotika als Wachstumsbeschleuniger bereits seit 1998 verboten. [12] Zusammen mit Schweden war sie darin Vorreiter in Europa. In Deutschland wurde das Verbot erst 2006 erlassen, in der EU 2008. Da Antibiotika als Wachstumsbeschleuniger aber in vielen Ländern nach wie vor erlaubt sind, entstehen auch weiterhin mehr und mehr resistente Bakterienstämme. Der internationale Waren- und Menschenverkehr sorgt dafür, dass sich diese resistenten Stämme überallhin verbreiten.
Der landwirtschaftliche Einsatz von Antibiotika wirkt sich auch auf das Mikrobiom in der Umwelt aus. Bis zu 90% der den Tieren verabreichten Antibiotika werden mit Urin und Stuhl ausgeschieden und dann über Dünger, Grundwasser und Oberflächenabfluss weit verbreitet. Zusätzlich werden in den westlichen und südlichen USA Tetracycline und Streptomycin auf Obstbäume gesprüht, um als Pestizide zu wirken. [13] Obwohl diese Anwendung einen viel geringeren Anteil des gesamten Antibiotikaeinsatzes ausmacht, kann die daraus resultierende geographische Ausbreitung beträchtlich sein.
Antibakterielle Produkte, die zu Hygiene- oder Reinigungszwecken verkauft werden, können ebenfalls zu dem Problem beitragen, da sie die Entwicklung von Immunitäten gegen pathogene Mikroben sowohl bei Kindern als auch bei Erwachsenen einschränken können. Folglich kann die Vielseitigkeit des Immunsystems beeinträchtigt werden, was möglicherweise die Morbidität und Mortalität aufgrund von Infektionen erhöht, die normalerweise nicht virulent wären. [14]
Entwicklung neuer Antibiotika (und bürokratische Hürden)
Die Entwicklung neuer Antibiotika ist ins Stocken geraten. [15] Die meisten Pharmaunternehmen haben den Antibiotikabereich abgegeben. Fusionen zwischen Pharmaunternehmen haben auch die Anzahl und die Vielfalt der Forschungsteams erheblich verringert. Die Entwicklung von Antibiotika wird nicht mehr als wirtschaftlich sinnvolle Investition für die pharmazeutische Industrie angesehen. Da Antibiotika nur für relativ kurze Zeiträume eingesetzt werden und häufig heilend wirken, sind Antibiotika nicht so rentabel wie Medikamente zur Behandlung chronischer Krankheiten wie Diabetes, psychiatrische Störungen, Asthma oder gastroösophagealer Reflux. [16]
Ein weiterer Faktor, der die Entwicklung von Antibiotika wirtschaftlich unattraktiv macht, sind die relativ niedrigen Kosten von Antibiotika. Die Verfügbarkeit, die einfache Anwendung und die allgemein niedrigen Kosten von Antibiotika haben auch dazu geführt, dass sie von den Kostenträgern und der Öffentlichkeit als wenig wertvoll empfunden werden.
Hinzu kommen die zu erwartenden Resistenzen auch gegen neuentwickelte Antibiotika. Da sich nicht vorhersagen lässt, wie lange ein Medikament wirksam bleiben wird, kann es sein, dass sich die Investition in ein neues Produkt kaum lohnt.
Was kann man tun?
Rasch auftauchende resistente Bakterien bedrohen die ausserordentlichen gesundheitlichen Vorteile, die mit Antibiotika erzielt wurden. Diese Krise ist global und spiegelt den weltweiten Übergebrauch dieser Medikamente und die mangelnde Entwicklung neuer Antibiotika durch die Pharmaunternehmen wider. Antibiotikaresistente Infektionen stellen eine erhebliche gesundheitliche und wirtschaftliche Belastung für Gesundheitssysteme in aller Welt dar. Koordinierte internationale Anstrengungen zur zu einer Lösung des Problems sind dringend erforderlich. Aber was kann man tun?
In einem Artikel aus dem Jahr 2015 veröffentlichte die Zeitschrift «Pharmacy & Therapeutics» Lösungsvorschläge [17]:
- Gezielte Schulung von Ärzten in der korrekten Verabreichung von Antibiotika
- Optimierung therapeutischer Verfahren
- Verbesserung der Diagnose und Diagnosewerkzeuge, um eine erregerspezifische Behandlung sicherzustellen
- Verbesserte Datenerhebung in Gesundheitswesen und Landwirtschaft sowie internationaler Datenaustausch, um dringende oder neu auftretende Antibiotikaresistenzen frühzeitig zu identifizieren und zu reagieren
- Aufklärung über bessere Prävention von bakteriellen Infektionen (Hygiene, Händewaschen)
- Regierungsinitativen und öffentlich-private Partnerschaften, um neue Anreize für die gewinnorientierte Arzneimittelentwicklung zu schaffen
- Weltweite Massnahmen zur Beschränkung des Antibiotikaeinsatzes in der Landwirtschaft.
[1] Gest H (2004): The discovery of microorganisms by Robert Hooke and Antoni Van Leeuwenhoek, fellows of the Royal Society. Notes Rec R Soc Lond. 2004 May;58(2):187-201.
[2] Sengupta S, Chattopadhyay MK, Grossart HP (2013): The multifaceted roles of antibiotics and antibiotic resistance in nature. Front Microbiol. 2013; 4():47.
[3] Aminov RI (2010): A Brief History of the Antibiotic Era: Lessons Learned and Challenges for the Future. Front Microbiol. 2010; 1: 134.
[4] WHO Website, 29 April 2019. https://www.who.int/news-room/detail/29-04-2019-new-report-calls-for-urgent-action-to-avert-antimicrobial-resistance-crisis. Accessed 7 May 2020.
[5] The antibiotic alarm. Nature. 2013;495(7440):141.
[6] Read AF, Woods RJ (2014): Antibiotic resistance management. Evol Med Public Health. 2014 Oct 28; 2014(1):147.
[7] The antibiotic alarm, 2013
[8] Bartlett JG, Gilbert DN, Spellberg B (2013): Seven ways to preserve the miracle of antibiotics. Clin Infect Dis. 2013;56(10):1445–1450.
[9] Gross M (2013): Antibiotics in crisis. Curr Biol. 2013 Dec 16; 23(24):R1063-5.
[10] Bartlett JG, Gilbert DN, Spellberg B (2013): Seven ways to preserve the miracle of antibiotics.
Clin Infect Dis. 2013 May; 56(10):1445-50.
[11] Golkar Z, Bagasra O, Pace DG (2014): Bacteriophage therapy: a potential solution for the antibiotic resistance crisis. J Infect Dev Ctries. 2014 Feb 13; 8(2):129-36.
[12] http://www.stvt.ch/wp-content/uploads/2016/02/Antibiotikamerkblatt-2015-korrigiert.pdf
[13] Gross, 2013
[14] Ventola CL (2015): The Antibiotic Resistance Crisis. Part 1: Causes and Threats. Pharmacy & Therapeutics. 2015 Apr; 40(4): 277–283.
[15] Bartlet et al, 2013
[16] Gould IM, Bal AM (2013): New antibiotic agents in the pipeline and how they can help overcome microbial resistance. Virulence. 2013 Feb 15; 4(2):185-91.
[17] Ventola CL (2015): The antibiotic resistance crisis: part 2: management strategies and new agents. Pharmacy & Therapeutics. 2015 May;40(5):344-52.


